Nh3'te hidrojen bağı bulunur mu?
Ammonyak (NH3) molekülündeki hidrojen bağları, fiziksel ve kimyasal özellikler üzerinde önemli bir etkiye sahiptir. Bu bağlar, NH3'ün su ile karışabilirliğini artırır, kaynama noktasını yükseltir ve moleküller arası düzeni sağlar. Ammonyakın çeşitli endüstriyel uygulamaları için kritik bir rol oynar.
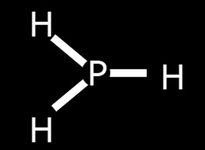
Nh3'te Hidrojen Bağı Bulunur Mu?Ammonyak (NH3), azot atomu ile üç hidrojen atomunun birleşiminden oluşan bir bileşiktir. Kimyasal yapısı itibarıyla, NH3'te hidrojen bağlarının varlığı, moleküller arası etkileşimler açısından önemli bir konu olarak karşımıza çıkmaktadır. Bu makalede, NH3'te hidrojen bağlarının varlığını ve bu bağların molekülün fiziksel ve kimyasal özelliklerine olan etkilerini inceleyeceğiz. Hidrojen Bağları Nedir?Hidrojen bağı, bir hidrojen atomunun, yüksek elektronegatifiteye sahip bir atom (genellikle fluor, oksijen veya azot) ile başka bir atom arasındaki etkileşimdir. Bu bağlar, zayıf elektrostatik çekim kuvvetleri ile oluşur ve moleküller arasında belirli bir düzenin sağlanmasına yardımcı olur. NH3 Molekülünde Hidrojen Bağları NH3 molekülü, azot atomu etrafında bulunan üç hidrojen atomu ile şekillenir. Azot, yüksek elektronegatif bir element olduğundan, NH3 molekülünde hidrojen atomları ile azot atomu arasında polar bir bağ oluşur. Bu polar yapı, molekülün dipol karakterini artırır ve dolayısıyla, NH3 molekülleri arasında hidrojen bağlarının meydana gelmesine neden olur.
NH3'ün Fiziksel Özelliklerine Etkisi NH3'teki hidrojen bağları, bileşiğin bazı fiziksel özelliklerini belirgin bir şekilde etkiler. Bu bağların etkisiyle, NH3'ün kaynama noktası ve erime noktası, benzer moleküllere göre daha yüksektir. Örneğin, metan (CH4) ile karşılaştırıldığında, NH3'ün kaynama noktası oldukça yüksektir. Bu durum, hidrojen bağlarının moleküller arası etkileşimleri artırmasıyla açıklanabilir. Sonuç Sonuç olarak, NH3 molekülünde hidrojen bağları bulunmaktadır. Bu bağlar, molekülün fiziksel ve kimyasal özelliklerini önemli ölçüde etkileyerek, ammonyak bileşiğinin çeşitli uygulamalarındaki rolünü artırmaktadır. NH3'ün hidrojen bağları, özellikle su ile etkileşimleri ve çözünürlük özellikleri açısından kritik bir öneme sahiptir. Ek Bilgiler |









.webp)