Hidrojenin izotopları nelerdir ve nasıl farklılık gösterirler?
Hidrojen, evrendeki en basit element olmasının yanı sıra üç farklı izotopa sahiptir: protyum, deuterium ve trityum. Bu makalede, bu izotopların özellikleri, aralarındaki farklar ve bilimsel uygulamaları detaylı bir şekilde ele alınacaktır. İzotopların kimyasal ve fiziksel özellikleri, birçok alanda önemli rol oynamaktadır.
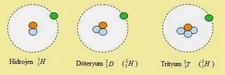
Hidrojenin İzotopları ve FarklılıklarıHidrojen, evrendeki en basit ve en hafif element olarak bilinir. Atom numarası 1 olan hidrojen, bir proton ve bir elektrondan oluşur. Bununla birlikte, hidrojenin üç farklı izotopu bulunmaktadır: protyum, deuterium ve trityum. Bu izotoplar, proton sayılarının aynı olmasına rağmen, nötron sayılarında farklılık gösterirler. Bu makalede, hidrojenin izotopları detaylı bir şekilde incelenecek ve bu izotopların birbirlerinden nasıl farklılık gösterdikleri açıklanacaktır. 1. Protyum (¹H) Protyum, hidrojenin en yaygın izotopudur ve doğal olarak bulunan hidrojenin yaklaşık %99.98'ini oluşturur. Protyum, bir proton ve bir elektrondan oluşur; yani, nötron içermez. Bu nedenle, protyum atomunun kütlesi en hafif hidrojen izotopudur. Protyum, kimyasal özellikleri açısından hidrojenin genel özelliklerini taşır ve çeşitli kimyasal reaksiyonlarda sıkça kullanılır. 2. Deuterium (²H)Deuterium, hidrojenin bir izotopu olup bir proton ve bir nötron içerir. Bu nedenle, deuterium atomunun kütlesi protyumdan yaklaşık iki kat daha fazladır. Deuterium, doğal hidrojenin yaklaşık %0.02'sini oluşturur ve su moleküllerinde de bulunabilir (örneğin, ağır su olarak bilinen D₂O). Deuterium, nükleer enerji, kimya ve biyokimya alanlarında çeşitli uygulamalara sahiptir. Ayrıca, deuterium zenginleştirilmiş su, nükleer reaktörlerde ve bazı araştırmalarda kullanılır. 3. Trityum (³H)Trityum, hidrojenin radyoaktif bir izotopudur. Bir proton ve iki nötron içerir, bu da onun kütlesini protyum ve deuteriumdan daha ağır hale getirir. Trityum doğal olarak çok az miktarda bulunur ve genellikle nükleer reaksiyonlar sonucu üretilir. Trityum, nükleer enerji uygulamalarında ve ışık kaynaklarında (örneğin, trityum içeren saatler) kullanılır. Ancak, radyoaktif özelliği nedeniyle trityumun kullanımı belirli güvenlik önlemleri gerektirir. İzotopların Farklılıkları Hidrojen izotopları, kimyasal ve fiziksel özellikleri itibarıyla bazı farklılıklar gösterir. Bu farklılıklar şunları içerir:
Sonuç Hidrojen, evrenin en temel elementlerinden biri olmakla birlikte, izotopları aracılığıyla farklılıklar sergilemektedir. Protyum, deuterium ve trityum, hidrojenin farklı özelliklere ve uygulamalara sahip olan izotoplarıdır. Bu izotopların incelenmesi, nükleer enerji, kimya ve biyokimya gibi alanlarda önemli katkılar sağlamakta ve bilimsel araştırmalara olanak tanımaktadır. Ayrıca, hidrojenin izotopları, okyanus ve atmosfer gibi doğal kaynaklarda da bulunarak, su döngüsü ve ekosistemler üzerinde etkili olmaktadır. |









.webp)