Hidrojen iyonik bağ oluşturabilir mi?
Hidrojen, basit yapısı ve kimyasal özellikleriyle dikkat çeken bir elementtir. İyonik bağ oluşturma yeteneği, çoğunlukla kovalent bağlar kurma eğiliminde olmasına rağmen, belirli koşullar altında gerçekleşebilir. Bu, hidrojenin kimyasal etkileşimlerindeki karmaşıklığı gösterir.
Hidrojen İyonik Bağ Oluşturabilir mi?Hidrojen, periyodik tabloda en basit ve en hafif element olarak yer almakta olup, kimyasal bağların oluşumunda önemli bir rol oynamaktadır. Bu makalede, hidrojenin iyonik bağ oluşturma yeteneği ve bunun arka plandaki kimyasal prensiplerle ilişkisi incelenecektir. Hidrojenin Kimyasal ÖzellikleriHidrojen, bir proton ve bir elektrondan oluşan basit bir atom yapısına sahiptir. Genellikle +1 oksidasyon durumuna sahip olup, diğer elementlerle etkileşime girdiğinde genellikle elektron kaybeder. Bu özellik, hidrojenin kimyasal bağ oluşturma kapasitesini belirleyen temel faktörlerden biridir.
İyonik Bağ Nedir? İyonik bağ, bir atomun diğer bir atomdan elektron alması sonucu oluşan elektrostatik çekim kuvvetine dayanan bir kuvvettir. Genellikle metal ve ametal elementler arasında görülmektedir. Metal atomları, elektronlarını kaybederek pozitif iyonlar (katyonlar) oluştururken, ametal atomları elektron kazanarak negatif iyonlar (anyonlar) oluştururlar.
Hidrojenin İyonik Bağ Oluşturma Yeteneği Hidrojen, tipik olarak iyonik bağ oluşturmak için uygun bir element olarak değerlendirilmez, çünkü çoğunlukla kovalent bağlar oluşturma eğilimindedir. Ancak, belirli koşullar altında hidrojen, diğer elementlerle birlikte iyonik bağlar oluşturabilir.
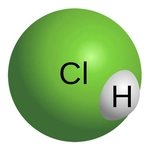
Örnekler ve Uygulamalar İyonik bağlar, hidrojenin bazı bileşiklerde nasıl yer aldığını anlamak için önemli örnekler sunmaktadır. Örneğin, hidrojen klorür (HCl) molekülü, hidrojenin bir ametal olan klor ile oluşturduğu kovalent bir bağdır. Ancak, sodyum hidrojen (NaH) gibi bazı bileşiklerde hidrojen negatif bir iyon (H⁻) olarak davranabilir ve bu durumda iyonik bir bağ oluşturur.
Sonuç Hidrojen, genellikle kovalent bağlar oluşturma eğiliminde olsa da, belirli şartlar altında iyonik bağlar da oluşturabilir. Bu, hidrojenin kimyasal özelliklerinin ve diğer elementlerle olan etkileşimlerinin karmaşıklığını göstermektedir. Dolayısıyla, hidrojenin iyonik bağ oluşturma kapasitesi, bağlandığı elementin özelliklerine ve çevresel koşullara bağlı olarak değişkenlik göstermektedir.
Bu bağlamda, hidrojenin kimyasal özellikleri üzerine daha fazla araştırma yapılması, hem teorik hem de pratik anlamda önemli sonuçlar doğurabilir. |









.webp)