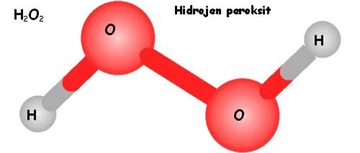
Hidrojen, döteryum ve trityum aynı elementin izotopları mı?
Hidrojen, dötaryum ve trityum, hidrojen elementinin izotoplarıdır ve farklı fiziksel özelliklere sahiptirler. Bu makalede, bu izotopların özellikleri, aralarındaki farklar ve kullanım alanları incelenecektir. Enerji üretiminden nükleer uygulamalara kadar geniş bir yelpazeye yayılmaktadırlar.
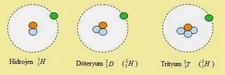
Hidrojen, Döteryum ve Tritiyum: Aynı Elementin İzotopları mı?Hidrojen, döteryum ve trityum, periyodik tablo içerisinde yer alan hidrojen elementinin izotoplarıdır. Bu makalede, bu izotopların özellikleri, farkları ve kullanım alanları üzerinde durulacaktır. İzotop Nedir?İzotoplar, aynı elementin atom numarası (proton sayısı) aynı ancak kütle numarası (proton ve nötron sayısının toplamı) farklı olan atomlarıdır. Bu durum, izotopların kimyasal özelliklerinin benzer olmasına rağmen fiziksel özelliklerinin farklı olmasına neden olur. Hidrojen ve İzotoplarıHidrojen, periyodik tabloda en hafif element olarak yer alır ve atom numarası 1'dir. Doğada üç ana izotop bulunur:
Hidrojen (Protiyum) Hidrojen, doğal olarak en yaygın bulunan izotoptur ve evrende en bol element olarak bilinir. Enerji üretiminde, kimyasal reaksiyonlarda ve birçok endüstriyel uygulamada kullanılır. Döteryum Döteryum, doğal hidrojenin yaklaşık %0.015'ini oluşturur. Nükleer reaktörlerde ve ağır su üretiminde önemli bir rol oynar. Döteryum, ağır su (D2O) formunda kullanıldığında, nötron moderatörü olarak işlev görür. Trityum Trityum, doğada nadir bulunan bir izotoptur ve radyoaktif bir yapıya sahiptir. Nükleer füzyon reaktörlerinde enerji üretimi için potansiyel bir kaynak olarak araştırılmaktadır. Ayrıca, trityum, ışık yayan bileşenlerde ve nükleer tesislerde güvenlik göstergeleri olarak da kullanılır. İzotopların Farklılıkları ve Kullanım Alanları Hidrojen, döteryum ve trityum arasındaki temel farklar, nötron sayısı ve dolayısıyla kütle numarasıdır. Bu farklılıklar, fiziksel ve kimyasal davranışlarını etkiler.
Sonuç Hidrojen, döteryum ve trityum, aynı elementin izotoplarıdır ve çeşitli fiziksel ve kimyasal özelliklere sahip olmaları nedeniyle farklı alanlarda kullanılmaktadır. Bu izotopların anlaşılması, nükleer enerji, kimya ve fizik alanlarında önemli bir rol oynamaktadır. Ekstra Bilgiler |









.webp)

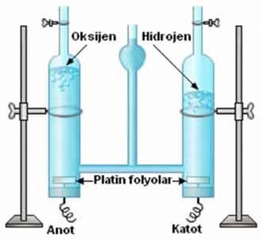



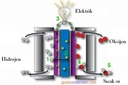


Hidrojen, döteryum ve trityumun aynı elementin izotopları olduğu bilgisi oldukça ilginç değil mi? Özellikle bu izotopların fiziksel ve kimyasal özelliklerinin farklılıkları, onların kullanım alanlarını da etkiliyor. Mesela, trityumun radyoaktif olması nedeniyle özel uygulamalarda kullanılması, dikkatli bir şekilde ele alınması gerektiğini gösteriyor. Ayrıca, döteryumun ağır su reaktörlerinde kullanılması da nükleer enerji alanında ne kadar önemli bir rol oynadığını ortaya koyuyor. Bu izotopların özelliklerini ve farklarını anlamak, bilimsel çalışmalarda ve endüstriyel uygulamalarda kritik bir öneme sahip gibi görünüyor. Sizce bu izotopların gelecekteki potansiyel kullanımları neler olabilir?
Kazan,
İzotopların Önemi
Hidrojen, döteryum ve trityumun izotop olması gerçekten de ilginç bir konu. Bu izotoplar, kimyasal ve fiziksel özellikleri bakımından önemli farklılıklar gösteriyor. Özellikle trityumun radyoaktif olması, onu belirli uygulamalarda dikkatli bir şekilde kullanılmasını gerektiriyor.
Gelecekteki Potansiyel Kullanımlar
Gelecekte, bu izotopların potansiyel kullanımları oldukça geniş bir yelpazeye yayılabilir. Örneğin, trityum, nükleer füzyon reaktörlerinde yakıt olarak kullanılabilir ve bu da enerji üretimi alanında büyük bir devrim yaratabilir. Ayrıca, döteryum, ağır su reaktörlerinde kullanılarak nükleer enerji üretiminde verimliliği artırabilir.
Bilimsel Araştırmalar
Bilimsel araştırmalarda, bu izotopların özelliklerini anlamak, yeni teknolojilerin geliştirilmesi için kritik bir adım olabilir. Ayrıca, tıpta ve biyolojik araştırmalarda, izotopların izleme ve tanı amaçlı kullanımları da artabilir.
Sonuç olarak, hidrojen izotoplarının gelecekteki potansiyel kullanımları, enerji üretiminden tıbbi uygulamalara kadar geniş bir alanı kapsıyor. Bu alanda yapılacak daha fazla araştırma, bu izotopların faydalarını daha da artırabilir.