Hidrojen Atom Numarası Nedir?
Hidrojen, periyodik tablonun en hafif ve en basit elementi olarak atom numarası 1 ile tanımlanır. Bu özellikleri, hidrojenin kimyasal davranışlarını ve farklı kullanım alanlarını etkiler. Enerji üretiminden, kimya endüstrisine kadar geniş bir yelpazede önemli bir rol oynar.
Hidrojen, periyodik tabloda en basit ve en hafif element olarak yer alır. Atom numarası, bir elementin periyodik tabloda yerini belirleyen ve o elementi tanımlayan temel bir özelliktir. Hidrojenin atom numarası 1'dir. Bu makalede, hidrojen atomunun özellikleri, atom numarasının önemi ve hidrojenin kimyasal davranışları üzerinde durulacaktır. Hidrojenin Temel Özellikleri Hidrojenin temel özellikleri arasında şunlar yer alır:
Atom Numarasının Önemi Atom numarası, bir elementin proton sayısını ifade eder. Proton sayısı, elementin kimyasal özelliklerini belirleyen en önemli faktörlerden biridir. Hidrojenin atom numarası 1 olduğundan, onun sadece bir protonu ve dolayısıyla bir elektronu vardır. Bu, hidrojenin oldukça reaktif olmasına ve diğer elementlerle kolayca bileşikler oluşturmasına olanak tanır. Hidrojenin Kimyasal Davranışları Hidrojen, çeşitli bileşiklerin oluşumunda önemli bir rol oynar. Kimyasal davranışları aşağıdaki gibi özetlenebilir:
Hidrojenin Kullanım Alanları Hidrojen, geniş bir kullanım yelpazesine sahiptir:
Sonuç Hidrojen, atom numarası 1 olan basit bir element olmasına rağmen, kimyasal özellikleri ve çok yönlü kullanımları ile dikkat çekmektedir. Hidrojenin atom numarası, onun temel yapısını ve reaktivitesini yansıtır. Bu nedenle, hidrojenin atom numarasını ve özelliklerini anlamak, hem teorik hem de pratik kimya alanında büyük bir önem taşımaktadır. Ekstra Bilgiler Hidrojen, evrenin en bol bulunan elementi olup, yıldızların ve gezegenlerin oluşumunda önemli bir rol oynar. Ayrıca, hidrojen, gelecekte sürdürülebilir enerji kaynakları arasında gösterilmektedir. Hidrojenin enerji depolama potansiyeli ve temiz enerji üretimindeki rolü, araştırmaların odak noktası olmaya devam etmektedir. |








.webp)






Hidrojen atom ağırlığı ile ilgili bir soru sormak istiyorum. Hidrojenin atom ağırlığı nedir ve bu, diğer elementlerle karşılaştırıldığında nasıl bir farklılık gösteriyor? Bu durum, hidrojenin evrendeki bol miktarda bulunmasına nasıl etki ediyor?
Hidrojenin Atom Ağırlığı
Hidrojenin atom ağırlığı yaklaşık olarak 1.008 u (atomik kütle birimi) civarındadır. Bu, hidrojen atomunun en hafif element olduğunu gösterir. Tek bir proton ve bir elektron içeren bu basit yapı, hidrojenin atom ağırlığını belirleyen temel faktörlerdendir.
Diğer Elementlerle Karşılaştırma
Hidrojen, diğer elementlerle karşılaştırıldığında oldukça hafif bir elementtir. Örneğin, karbonun atom ağırlığı yaklaşık 12.01 u, oksijenin ise yaklaşık 16 u'dur. Bu büyük fark, hidrojenin atom yapısının daha basit olmasından kaynaklanmaktadır. Bu durum, hidrojenin evrende çok yaygın olmasının sebeplerinden biridir; daha düşük bir atom ağırlığına sahip olması, evrende daha fazla sayıda hidrojen atomunun var olmasına olanak tanır.
Hidrojenin Evrendeki Bol Miktarda Bulunması
Hidrojenin bu kadar yaygın olmasının bir diğer nedeni, Big Bang sonrası evrenin ilk oluşum aşamalarında en basit ve en hafif elementin hidrojen olmasıdır. Yıldızların oluşum süreçlerinde, hidrojen atomları birleşerek daha ağır elementleri oluştururlar. Ancak, hidrojenin kendi varlığı, yıldızların ve galaksilerin oluşumunda temel bir rol oynar. Bu nedenle, hidrojenin atom ağırlığı ve yapısı, onun evrendeki bol miktarda bulunmasına önemli ölçüde katkıda bulunmaktadır.
Hidrojenin periyodik cetveldeki yeri ve özellikleri hakkında okuduklarım beni düşündürdü. Acaba hidrojen alkali metal mi? Çünkü bazı özellikleriyle alkali metallere benziyor gibi görünüyor, ama farklı bir grupta yer alıyor. Bu çelişkiyi anlamak ilginç!
Hidrojenin Periyodik Cetveldeki Yeri
Hidrojen, periyodik cetvelde 1. grup ve 1. periyotta yer alır. Özellikle alkali metallerin bulunduğu grup ile aynı hizada olmasına rağmen, kimyasal ve fiziksel özellikleri bakımından onlardan farklıdır.
Hidrojenin Özellikleri
Hidrojen, alkali metallere benzer bazı özellikler gösterir; örneğin, su ile tepkimeye girdiğinde hidrojen gazı açığa çıkararak bazik özellikler sergileyebilir. Ancak, hidrojenin en belirgin özelliği, gaz halinde bulunması ve çok hafif olmasıdır. Alkali metaller genellikle katı halde bulunur ve su ile temas ettiklerinde oldukça reaktiftir.
Çelişki ve Farklılıklar
Hidrojen, elektron düzeni açısından alkali metallere benzemekle birlikte, temel farklılıkları vardır. Alkali metaller, metalik özellikler gösterirken hidrojen, ametal bir elementtir. Ayrıca, hidrojenin kimyasal davranışları alkali metallere göre daha çeşitlidir; asidik, bazik ve nötral özellikler gösterebilir.
Sonuç olarak, hidrojenin periyodik cetveldeki yeri ve özellikleri, onun hem alkali metallere benzer yönleri hem de onlardan farklı olan özellikleri ile bilimsel bir merak uyandırmaktadır. Bu durum, kimya biliminin karmaşıklığını ve elementlerin çeşitliliğini de gözler önüne seriyor.
Hidrojenin kütle numarası, atom yapısının temelini oluşturur. Bu bağlamda, hidrojenin kütle numarasının 1 olduğunu unutmamak gerekir. Bu özellik, hidrojenin diğer elementlerle olan etkileşimlerinde ve bileşenlerinde belirleyici bir rol oynamaktadır. Bu yüzden hidrojenin kütle numarası önemlidir.
Değerli Özata,
Hidrojenin kütle numarasının 1 olması, gerçekten de atom yapısı ve kimyasal etkileşimler açısından son derece önemli bir noktadır. Bu özellik, hidrojenin diğer elementlerle olan bağlarını ve bileşenlerini şekillendiren temel bir unsurdur. Ayrıca, hidrojenin evrende en yaygın elementlerden biri olduğunu düşündüğümüzde, bu kütle numarasının kimya ve fizik alanındaki yeri daha da anlam kazanıyor.
Hidrojenin kütle numarasının 1 olması, onu diğer elementlerle karşılaştırıldığında oldukça hafif bir element yapar. Bu özellik, hidrojenin gaz halindeki davranışını ve reaktifliğini de etkiler. Örneğin, hidrojenin çeşitli bileşiklerde yer alması, onun bu özelliklerinden kaynaklanır.
Sonuç olarak, hidrojenin kütle numarasının önemi, sadece atomik düzeyde değil, aynı zamanda kimyasal süreçlerdeki rolü açısından da büyüktür. Bu konudaki düşünceleriniz ve derinlemesine analiziniz için teşekkür ederim.
Hidrojen atom numarası 1 olan en basit elementtir. Doğada yaygın olarak bulunması ve diğer elementlerle bileşikler oluşturma yeteneği, onun önemli bir rol oynamasına neden oluyor. Peki, hidrojenin atom numarası bu kadar düşük olmasına rağmen evrendeki etkisi nasıl bu kadar büyük?
Hidrojenin Önemi
Hidrojen, evrenin en basit ve en hafif elementi olmasının yanı sıra, evrendeki en bol bulunan elementtir. Bu durum, hidrojenin yıldızların oluşumunda ve enerji üretiminde kritik bir rol oynamasına olanak tanır. Yıldızlar, hidrojen atomlarını birleştirerek helyum oluşturur ve bu süreçte büyük miktarda enerji açığa çıkar. Bu enerji, yıldızların ışımasını ve evrendeki birçok süreçte enerji kaynağı olmasını sağlar.
Kimyasal Bileşenler
Hidrojenin atom numarasının düşük olması, onun diğer elementlerle kolayca etkileşime girmesine yardımcı olur. Bu da, su gibi hayati bileşenlerin yanı sıra, organik bileşenlerin oluşumuna da katkıda bulunur. Su, yaşamın temel taşlarından biri olduğu için hidrojenin varlığı, yaşamın varlığında doğrudan etkili olmuştur.
Evrenin Yapısı
Hidrojen, evrenin ilk oluşum anlarında büyük miktarda bulunan bir elementtir ve bu, evrendeki galaksilerin ve yıldızların gelişiminde önemli bir rol oynamıştır. Dolayısıyla, atom numarası 1 olan bu basit element, evrendeki karmaşık yapıları ve yaşamın temel unsurlarını şekillendirmede büyük bir etkiye sahiptir.
Sonuç olarak, hidrojenin basit yapısı ve evrendeki yaygınlığı, onun önemli bir element olmasını sağlamakta ve birçok süreçte başrol oynamasına olanak tanımaktadır.
Hidrojenin doğada oldukça yaygın bir element olduğunu biliyor muydunuz? Özellikle suyun oluşumunda en temel bileşen olarak karşımıza çıkıyor. Su, yaşamın temel kaynağı olduğu için hidrojenin bu rolü gerçekten çok önemli. Ayrıca, hidrojenin laboratuvar ve sanayideki üretim yöntemleri de dikkat çekici; özellikle hidrokarbonların su buharı ile tepkimeye girmesi oldukça ilginç. Hidrojenin, canlıların vücudundaki oranı da düşündürücü; vücudumuzun %10'unu oluşturması onun ne kadar hayati bir element olduğunu gösteriyor. Bunun dışında, hidrojenin izotopları hakkında ne düşünüyorsunuz? Protium, Deuterium ve Tritium'un fiziksel özellikleri arasındaki farklılıklar bilimsel araştırmalar açısından büyük bir potansiyele sahip gibi görünüyor.
Hidrojenin Önemi
Evet, Berksoy, hidrojenin doğada yaygın bir element olduğunu ve suyun oluşumundaki kritik rolünü bilmek gerçekten önemlidir. Su, yaşamın temel kaynağı olarak kabul ediliyor ve hidrojen, bu bileşiğin en önemli bileşenidir. Bu nedenle, hidrojenin varlığı ve rolü, yaşamın devamı açısından hayati bir öneme sahiptir.
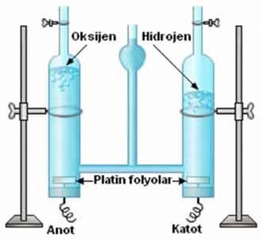
Üretim Yöntemleri
Hidrojenin laboratuvar ve sanayideki üretim yöntemleri, özellikle hidrokarbonların su buharı ile tepkimeye girmesi gibi süreçler, gerçekten ilgi çekici. Bu yöntemler, enerji üretimi ve çeşitli endüstriyel uygulamalar için oldukça değerli olabilir.
Vücutta Hidrojen Oranı
Ayrıca, hidrojenin insan vücudundaki oranı da dikkat çekici; vücudumuzun %10'unu oluşturması, onun ne kadar hayati bir element olduğunu gösteriyor. Bu durum, hidrojenin biyolojik sistemlerdeki rolünü daha da önemli hale getiriyor.
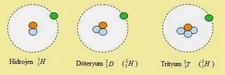
İzotoplar Üzerine Düşünceler
Hidrojenin izotopları olan Protium, Deuterium ve Tritium arasındaki fiziksel özellikler, bilimsel araştırmalar açısından büyük bir potansiyele sahip. Bu izotopların farklı özellikleri, enerji üretimi, tıbbi uygulamalar ve diğer birçok alanda yeni keşiflerin kapısını aralayabilir. Bu konudaki gelişmeleri takip etmek, bilimsel merakınızı daha da artırabilir.